
1. 아미노산의 산과 염기의 성질에 대해 알아보고 그 성질을 통해 아미노산을 적정한다. 미지의 아미노산을 적정하여 그 결과를 보고 미지의 아미노산을 확인한다. 또한 이를 통해 등전점에 대해 이해한다.
2. 1가지의 완충용액과 3가지의 아미노산을 적정하여, 이 아미노산의 pH 변화를 그래프로 그려, 시료가 어떤 아미노산이었는지 측정하고, 아미노산의 특성에 대해 이해해보도록 한다.
3. 아미노산의 pKa는 수용액 내의 짝산과 짝염기의 농도가 같을 때의 pH라는 것은 Henderson - Hasselbalch equation을 살펴보면 알 수 있다. 적정곡선 상에서 보면 염기를 가하여도 pH가 그다지 변화하지 않는 변곡점에서의 pH가 아미노산의 pKa이다. 이렇게 아미노산 용액을 염기성 용액으로 적정하면 적정곡선을 통해서 당량점과 pKa를 찾을 수 있다.
4. 본 실험에서는 aspartic acid, phenylalanine, lysine 3가지 아미노산에 대하여 NaOH 용액으로 적정한 그래프를 얻어, 각 아미노산의 pKa값과 당량점을 구하고 실험에 쓰인 아미노산을 알아낸다
산 염기 적정
적정은 농도를 알고 있는 물질 A의 용액을 농도를 알지 못하는 물질 B의 용액에 가해 정량적으로 반응이 일어나게 한 후, 반응을 완결시키는데 들어간 물질 A의 농도를 계산하여 물질 B의 농도를 알아내는 일이다. 산과 염기가 반응하면 정량적으로 중화되어 염과 물이 생긴다.
HCl + NaCl → NaCl + H2O
H2SO4 + Ba(OH)2 → BaSO4 + 2H2O
일정량의 산이 완전히 중화되려면, 이와 똑같은 당량의 염기가 필요한데, 산과 염기가 같은 당량끼리 반응한 점을 당량점이라 한다. 중화반응이 완전히 끝나는 종말점의 수소이온 농도를 지시약을 써서 관찰함으로써 화학 양론적 중화점인 당량점을 알 수 있다.

미지용액에 표준용액을 가하면서, 지시약이 변하는 순간을 포착하여, 측정․계산하면 미지용액의 농도를 알 수 있다. 이러한 방법을 중화적정이라고 하고, 지시약은 다음과 같다.
아미노산
단백질은 아미노산들의 탈수 중합체(dehydration polymer)로서 각 아미노산 잔기는 독특한 공유결합에 의해 다음 아미노산과 결합되어질 때 물분자가 소실됨을 의마한다. 단백질은 여러 가지 방법에 의해서 그의 구성성분이 되는 아미노산으로 분해할 수 있다.
아미노산(amino acid)은 단백질의 구성단위로 화학적 전달자(chemical messenger)로서 이용된다. 아미노산은 화학적 전달자로서 트립토판으로부터 유래된 serotonin이나 GABA인 신경전달물질, 혹은 티로신으로부터 유래된 thyroxine 등의 호르몬으로 작용한다. 또한 아미노산은 다양한 분자의 전구체이며, 특히 nucleotide, heme, cytochrom 등의 질소화합물의 출처라 할 수 있으며, 대사물질의 중간물질로서 사용된다.
아미노산은 부제탄소(chiral C)에 카르복실기와 아미노기가 결합된 일반 구조를 갖는다. 이 구조 중 카르복실기와 아미노기가 해당 아미노산이 존재하는 용액의 pH에 따라 존재하는 형태를 변화시킴으로써 염기성이나 산성, 중성으로 작용하기도 한다. 따라서 아미노산은 양쪽성 이온이라 할 수 있다.
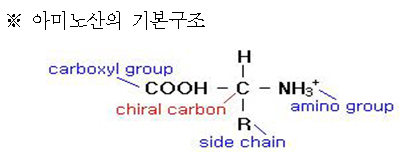
아미노산은 L형이나 D형으로 존재한다. 이 두 구조는 구조이성체의 관계이며, 체내에 존재하는 단백질은 모두 L형이지만 자연계에는 D형도 존재한다. 아미노산은 R로 표시되는 곁사슬의 종류에 따라 구분되며, 물과 작용하는 성질에 따라 중성의 무극성, 중성의 극성, 산성, 염기성의 4가지로 분류한다.
실험 방법
1. 실험 과정
① pH가 4.01인 용액과, 10.01인 용액을 이용해서 pH meter보정, autoshutoff 장치 끄기(pH meter에 Ready라는 글자가 떴을 때 수치를 읽는다.)
② 실험은 4인 1조로 하고 1조당 pH meter 1개, amino acid 2개씩 한번씩 만 적정한다
③ 준비조는 원액 amino acid solution을 10㎖씩 취해서 100㎖로 묽힌다
④ 0.2M NaOH 용액을 2조당 250㎖ 제조(한번 적정시 NaOH solution 25㎖ 정도 사용)
⑤ NaOH 용액으로 buret을 헹군 뒤, 50㎖의 NaOH를 buret에 넣는다.
⑥ 미지의 아미노산 용액 50㎖을 비이커에 담고, NaOH 용액을 1㎖ 간격으로 떨어뜨리면서 pH meter를 이용하여 pH를 측정한다.(처음에 약 7~10㎖의 NaOH 용액을 넣어준다.)
⑦ 이때 사용한 염기의 부피와 그때의 pH에 대한 값을 얻는다(pH 12까지 측정)
⑧ 계속해서 1㎖ 씩 HCl 용액을 첨가해가며 pH가 1.5근처에 이를 때까지 pH를 측정 한다.
⑨ 여기서 얻은 data를 이용해서 각각에서 대략적인 pKa값과 당량점 그리고 사용한 아미노산의 종류를 알아본다.
[생화학실험]아미노산의 적정(Amino Acid Titration)
[생화학실험]아미노산의 적정
educhemup.blogspot.com
[생화학 실험]아미노산의 적정 레포트
1. 실험 목적 (1) 아미노산의 산과 염기의 성질에 대해 알아보고 그 성질을 통해 아미노산을 적정한다. 미지의 아미노산을 적정하여 그 결과를 보고 미지의 아미노산을 확인한다. 또한 이를 통해 등전점에 대해 이해한다. (2) 1가지의 완충용액과 3가지의 아미노산을 적정하여, 이 아미노산의 pH 변화를 그래프로 그려, 시료가 어떤 아미노산이었는지 측정하고, 아미노산의 특성에 대해 이해해보도록 한다. (3) 아미노산의 pKa는 수용액 내의 짝산과 짝염기의 농
www.happycampus.com


댓글