1. 물 위에 생기는 기름막을 이용해서 몰(㏖)을 정의하는데 필요한 아보가드로 수를 결정한다.
2. 헥산과 스테아르산의 1㎖당 방울수를 측정해, 화학에서 자주 다루는 ㏖에 대해 자세히 알아본다.
3. 스테아르산은 물 표면에 퍼지면서 단막층을 형성하는데, 이 성질을 이용하면 탄소 1몰에 들어 있는 원자 수와 탄소 원자 1개가 얼마나 큰 가를 예상할 수 있다. 즉, 이 실험을 통해 아보가드로 수를 실험적으로 구할 수 있다.
4. 친수성과 소수성을 모두 갖는 스테아르산이 물 표면에서 퍼지면서 단분자막을 형성하는 성질과 다이아몬드의 밀도를 이용해서 몰(㏖)을 정의하는데 필요한 아보가드로수를 결정한다.
아보가드로수
화학에서 원자나 분자는 매우 작은 입자이기 때문에 하나의 질량을 직접 측정하는 것은 매우 어렵다. 따라서 원자나 분자를 일정수로 묶어서 측정하고 그 묶음을 1몰(mole)이라고 약속하면 해결가능하다. 탄소 12g에는 탄소원자가 6.02×1023 개가 있고 이를 1묶음, 즉 1몰이라고 정의하면 다른 분자들도 이 수만큼의 질량을 결정할 수 있다.
이렇게 기체에 관한 아보가드로의 법칙으로부터 결정되었고, 분자뿐만 아니라 이온·원자 등으로 되어 있는 모든 물질(고체 및 액체도 포함)에 대해 적용할 수 있다는 사실이 알려졌다. 아보가드로수는 보통 으로 표시하며 첨자 A는 아보가드로(Avogadro)의 첫 글자를 따온 것이며 이 수를 아보가드로수(Avogadro's number, NA=6.022×1023 )라고 한다. 이것은 마치 연필 12개를 1다스라고 부르는 것과 마찬가지이다. 다만 원자나 분자는 그 크기와 질량이 매우 작기 때문에 아보가드로수가 대단히 크게 느껴질 뿐이며 이 수만큼 묶어 놓은 원자량이나 분자량은 아주 유용하게 사용 된다.
이 값은 1865년 오스트리아의 로슈미트가 처음으로 결정했으며, 한때 아보가드로수를 로슈미트수라고 한 일도 있다. 그러나 지금은 국제적으로 아보가드로수라 하고, 표준상태 1㏖의 기체 속에 존재하는 분자의 수를 22400으로 나눈 N/22400을 로슈미트수라 하여 구별하고 있다.
다음 정보를 이용하면 실험을 통해 아보가드로수를 확인할 수 있다. 아보가드로수는 탄소 원자 1몰이 차지하는 부피(Vm)와 탄소 원자 하나가 차지하는 부피(Vm)를 알면 다음 식을 이용해서 얻을 수 있다.
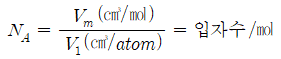
예를 들면 물(H2O)는 전자를 잘 잡아당기는 산소 한 개에 두 개의 수소가 104.5의 각도를 이루며 결합되어 있어서 전기쌍극자의 성질을 갖고 있는 극성 분자이다. 액체 상태에서 물 분자의 이런 극성은 전하를 가진 양이온과 음이온은 물론이고 다른 극성 분자를 안정화시켜서 잘 녹게 만들어준다. 소금(NaCl)이 물에 잘 녹는 것도 바로 물의 이런 특성 때문이다. 그러나 전기쌍극자의 성질을 갖지 않는 벤젠이나 헥산과 같은 무극성 분자들은 물과 잘 섞이지 않는다.
아보가드로수를 얻는 방법은 라듐의 α붕괴에 의한 헬륨 생성량을 측정하여 구하는 방법, 밀리컨의 기름방울실험을 이용한 기본전하량(基本電荷量)의 결정 및 전기분해로부터 얻은 패러데이상수를 함께 써서 구하는 방법 등이 있다. 또 정밀도가 높은 방법으로 결정(예컨대 다이아몬드)의 단위격자를 X선 해석에 의해 정확히 결정한 다음, 그 속의 원자수를 구하는 방법이 있다.
실험 방법
1. 스포이트 보정(피펫 보정)
1) 헥산으로 여러 차례 헹군 스포이드에(피펫눈금까지) 헥산을 충분히 채운다.
2) 스포이드를 수직으로 세워 눈금실린더에 헥산을 반쯤 채우고 눈금을 읽고, 헥산 용액을 한 방울 씩 떨어뜨려 1.00㎖를 채우면서 떨어지는 방울수를 센다. 만약, 1.00㎖의 방울 수가 100이하이면 구멍이 더 작은 스포이드로 바꾸어야 한다. 이 과정을 여러번 되풀이하여 오차가 4~5방울 내에 들면 좋다. 피펫을 잡는 각도가 방울 수와 방울의 크기에 영향을 주는데 수직에서 45°벗어나면 30% 정도 방울 수가 적어짐을 알아야 한다.
3) 이 과정을 2회 반복하여 하여 평균을 구한다.
2. 스테아르산 단막층의 표면적 측정
1) 시계접시를 보관액에서 꺼내 흐르는 물로 깨끗이 씻고 휴지를 이용해 잘 닦은 다음 접시의 직경을 측정한다.
2) 깨끗한 시계접시의 가장자리까지 증류수를 붓는다. 증류수를 가득 부으면 표면장력에 의해 가운데 부분이 동그랗게 올라오는데, 휴지를 이용하여 증류수 표면이 수평이 되게 한다. 이때 가장자리의 빈틈이 없도록 채우는데 옆에서 봤을 때 볼록해질 때까지 붓는다.
3) 작은 약 숟가락으로 송화가루를 조금 떠서 시계접시의 가운데 부분에 조심스럽게 뿌려 준다. 송화가루가 시계접시의 벽에 닿지 않게 원형으로 퍼지도록 한다.
4) 0.01 ~ 0.02g정도의 스테아르산을 헥산 100㎖에 녹인 용액을 스포이드에 넣어서 한 방울을 송화 가루가 퍼져 있는 시계접시위에 떨어뜨린다. 스테아르산이 퍼지면서 생기는 원형 기름막의 경계면을 쉽게 구별할 수 있을 것이다.
5) 원형으로 퍼진 단분자층의 직경을 측정한다. 원형이 아닌 경우에는 대각선 방향의 길이를 여러번 측정해서 평균값을 얻는다.
6) 이 과정을 3회 반복하여 평균을 구한다.
7) 다 사용한 시계접시는 깨끗이 세척한 후 물기를 제거하여 비커 안에 준비된 세정액에 담그고, 피펫은 스테아르산 용액으로 여러 번 씻어낸다.
[일반화학실험]아보가드로 수의 결정 1부
[일반화학실험]아보가드로 수의 결정 1부
educhemup.blogspot.com
[일반화학실험]아보가드로 수의 결정 레포트
실험 원리 및 이론 (1) 화학에서 원자나 분자의 수는 어떻게 셀 수 있나? 분자의 실제 크기를 측정하고 이를 이용하여 1몰에 존재하는 분자의 수를 결정하여 아보가드로 수를 확인하고자 한다. 실험에서 스테아르산 분자의 길이를 측정하게 되는데 이 물질은 비누와 같은 화합물이다. 스테아르산 분자의 한 쪽 끝은 친수성을 갖는 카르복실기를 가지고 있으며 다른 쪽 끝은 비극성인 탄화수소 사슬로 이루어진 기름분자를 가지고 있다. 따라서 거의 녹지 않는다. 이런 형태
www.happycampus.com


댓글