생물학적 검정법 (biological assay) 과 in vitro 악리 시험
약물을 생체에 투여하고 그때 나타나는 동물의 전체 또는 부분적 반용을 관찰하여 그 약물의 정량적 또는 정성적 생리활성 (biological activity) 를 추정하는 실험을 생물학적 검정법이라 하는데 생약제제, 호르몬제제, 혈청제제 또는 항생제 동의 분석이나 약물의 효능 평가에 사용된다. 또, 동 · 식물 중에 존재하는 유용한 약효성분을 유리하려고 할 때도 추출 과정에서 이러한 검정법을 이용해서 그 성분을 추적한다.
일반적으로 물리, 화학반응은 반옹조건을 엄격하게 조정함으로써 실험 오차를 줄이고 높은 재현성을 얻을 수 있으나, 생물반옹에 있어서는 그러한 조정이 용이치 못하다. 완전히 동일한 두 사람이 존재하지 않는 것과 같이, 약리실험에 사용하는 한 종의 동물도 외견상으로는 같아도 개체간에는 상당한 차이가 있다. 때로는 체중의 차이, 성별 그리고 그들이 취하는 먹이 등에 따라 생리반응의 현격한 차이가 나타날 수 있기 때문에 동물을 대상으로 한 실험에서는 많은 실험오차가 존재한다. 따라서 일반적으로 생물반옹의 실험에서는 동일한 실험에 많은 수의 동물을 사용하여 반복하고, 얻은 결과를 통계학적으로 처리함으로써 의미있는 실험결과를 얻을 수 있다.
독성시험은 신약개발에서 가장 중요한 시험 중의 하나이다. 이 실험에서는 흔히 LD50라고 부르는 평균 치사량(median lethal dose) 을 얻는데, 이는 사용한 동물의 50 %가 치사하는 데 소요되는 약물의 용량으로서 mg/kg으로 표시된다. 이때 충분히 다수의 동물을 사용하면 그 도수분포가 그림 1과 같은 정규형이거나 또는 이와 근사한 곡선으로 나타나는데 평균치 M이 LD50에 해당한다. 그러나 실제로 다수의 동물을 사용한다는 것은 여러 면에서 비경제적이므로 유의한 중간치와 신뢰한도를 얻는 범위 내에서 가능한 소수의 동물을 사용함이 바람직하다고 하겠다.
그림 1 에서 중간치 M과 표준편차 σ 는 다음과 같은 식으로 산출되는데,
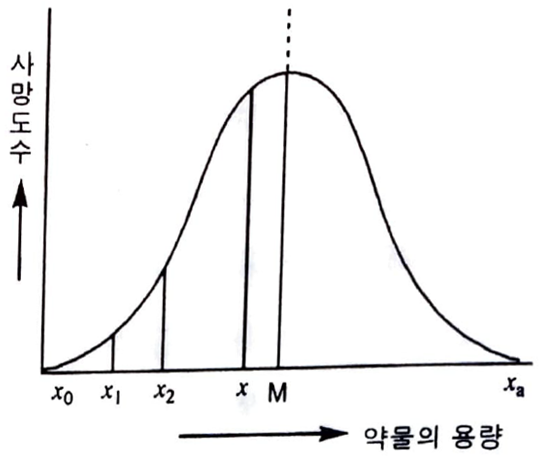
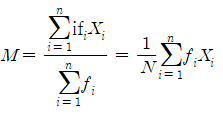
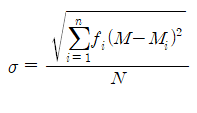
여가서, Xi(각 약물 용량의 중앙치, fi. : 각 약물 용량에서의 사망도수, N: 전체 동물수
단, n( 또는 N) 의 수가 적을 때, 즉 약효검색이나 기초약리실험에서 같이 사용하는 동물의 수가 20을 넘지 않는 경우에 있어서는 표준편차( n 의 수가 적을 때는 표준편차는 보통 s 로 표시한다)는 다음과 같은 식으로 구한다.
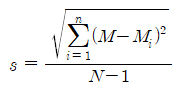
생물반응을 통계학적으로 처리하는 데는 계수적 반응(quantal response 또는 all or none response) 과 계량적 반응(quantitative response) 의 두 가지 방법이 있는데, 전자 에서 는 생리 반응을 생사 여부, 경련 발생 여부 둥과 같이 그 출현의 유무로서 취급하며 + 또는 -로 표시하여 결과를 판정의 지표로 삼는다. 이때 반옹의 강약 정도는 고려되지 않는다. 일반적으로 계수로 취급되는 LD 또는 ED 등이 이에 속한다. 이에 반하여 후자인 계량적 반옹은 반옹을 그 강도에 따라 수치로 표현한다. 일반적으로, 약리실험에서는 계량적 반옹에 의한 검정법이 선호되는데, 이는 계수적 방법보다 실험 정밀도가 높기 때문이다.
생체 내에서의 약물효과는 약물의 흡수, 분배, 대사 등 여러 요인이 복합적으로 작용하여 나타나는 종합적 반옹이다. 어떤 약물이 체내 어느 특정기관이나 조직에 미치는 생리작용을 규명하기 위해서는 그 기관이나 조직을 유리하여 이를 약물과 작용시킨다. 이런 목적으로 가장 흔히 사용되는 조직 중의 하나가 소장(small intestine) 인데, Mognus 에 의하여 처음으로 사용되었다.
소장의 작은 조각(2~5 cm) 을 혈장(blood plasma) 의 이온농도와 비슷한 소금물에 담그고 생체 온도와 비슷한 온도 하에서 산소를 불어넣어 주면 그 장기는 몇 시간 동안 계속 약물에 대하여 반응을 나타낸다. 그림 2 는 그러한 소장 조각이 약물에 의하여 수축하거나 이완하는 것을 측정하는 장치를 도시한 것이다. 그림에서 보는 바와 같이 소금물에 잠긴 소장 조각의 한쪽 끝온 지랫대에 매달고 다른 쪽 끝은 고정시켜 놓은 후 근육을 수축시키는 약물을 용액에 가하면 그 조각은 수축을 일으키고 이것이 지랫대를 통하여 도면 (chart) 에 나타난다.

실제로 이 수조에 아세틸콜린(acethylcholine) 이라는 신경전도물질(neurotrasmitter)을 가하면 그 소장 조각은 2~3초 내에 수축반응을 나타낸다. 그러나 그 용액을 제거하고 새로운 용액을 넣어 주면 그 수축되었던 소장은 다시 원상태로 돌아간다. 만약 아세틸콜린의 농도를 충분히 낮추어 주면 그의 근육 수축 효과는 나타나지 않게 된다.
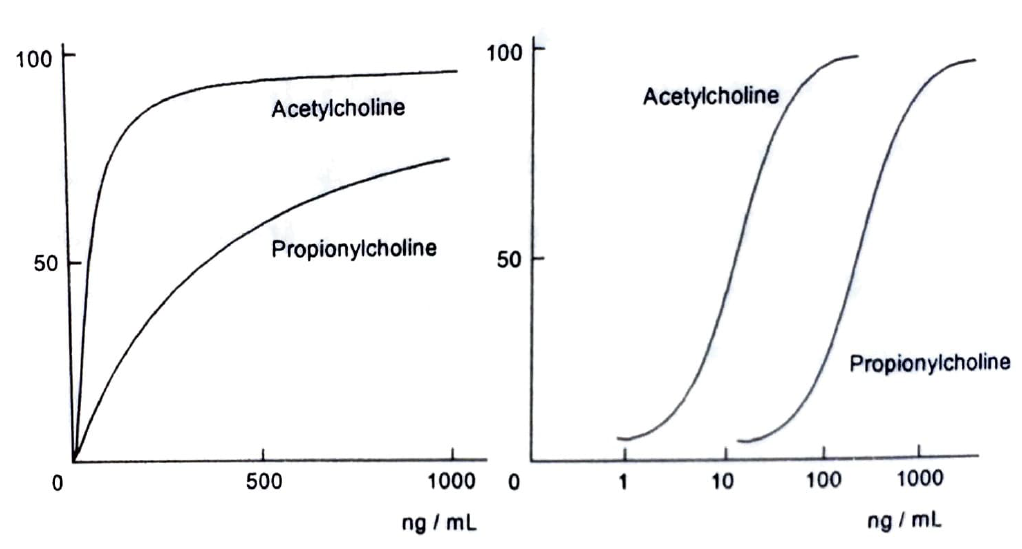
이 상태에서 아세틸콜린의 농도를 단계적으로 서서히 증가시키면 수축의 정도도 또한 농도의 증가와 더불어 증가하다가 어느 일정 농도에 도달하면 그 이상 더 수축의 증가가 일어나지 않는 것을 볼 수 있다. 이 실험에서 아세틸콜린의 농도와 소장의 수축반웅과의 상관관계를 도표로 표시하면 그림 3와 같이 나타나는데 이를 용량-반응 곡선(dose-response curve)이라고 칭한다.
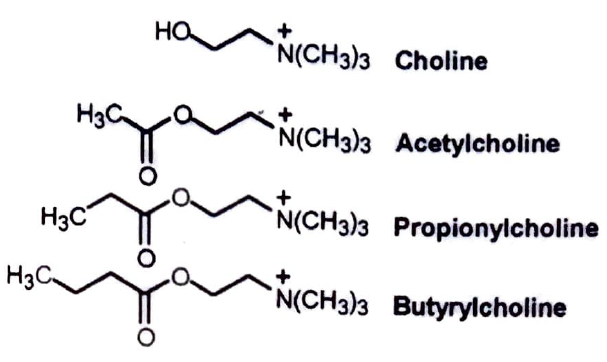
아세틸콜린은 체내에서 미량으로 존재하는 물질이며 이의 분자 구조를 살펴보면 암모늄염인 콜린의 아세트산 에스테르 임을 알 수 있다 . 이러한 물질이 근육 수축 효과를 나타내기에 필요한 분자구조의 특성을 알아보는 한 방법은 아세틸콜린의 동족체 (homolog) 들이 또한 아세틸콜린과 같은 생리효과를 나타내는가를테스트하여 보는 것이다.
실제로 그러한 목적으로 합성된 여러 동족체들 중에서 프로피오닐콜린(propionylcholine) 과 같은 물질은 소장의 일부를 사용한 그림 2 와 같은 실험에서 아세틸콜린과 비슷하게 용량에 비례하여 수축 반옹을 일으키고, 어느 일정한 농도에 달하게 되면 프로피오닐콜린을 더 가하더라도 그 이상 수축이 증가하지 않는 최대 수축 상태에 도달하는 것을 관찰할 수 있었다. 이의 용량-반응 상관관계는 그림 3 의 아래 곡선과 같이 표현된다.
이 두 물질들의 생리효과를 비교할 때 차이점은 프로피오닐콜린으로서 아세틸콜린과 같은 정도의 수축을 야기시키려면 약 20 배 정도의 더 높은 농도가 필요하다는 것이다. 이것은 프로피오닐콜린이 완전 효능약(full agonist) 이라는 것을 의미하는데, 여기서 완전이란 말은 이것이 아세틸콜린과 비교해서 동등한 최대 수축 효과를 나타낸다고 하는 뜻이다. 그러나 프로피오닐콜린의 효력 (potency) 은 아세틸콜린의 5 %에 불과하다.
이러한 관계는 아세틸콜린의 다른 동족체에서도 볼 수 있다. 이들의 용량-반응 곡선(그림 3) 을 볼 때 왼쪽의 것은 횡축으로 용량을 표시하고 종축은 최대 수축의 백분율로서 생리반옹의 정도를 표시한 것이다. 아세틸콜린의 경우 이때 나타나는 곡선은 삼각 쌍곡선 (rectangular hyperbola) 의 형태이다. 그러나 이 곡선은 좌표의 왼쪽으로 압축되어 있으며, 또 프로피오닐콜린의 경우는 상하가 잘 표시되어 있지 않다. 이 그림에서 2 개의 곡선이 유사하다는 것은 얼른보아서는 감지하기 힘들다. 오른쪽의 그림은 사용 시료의 용량을 횡축에 로가리즘 척도 (logarithm scale)로 표시한 것인데 이렇게 처리하게 되면 상관관계를 나타내는 곡선이 S 형의 대칭 곡선으로 표시되며 사용한 모든 용량의 프로피오닐콜린이 그래프 내에 들어갈 수 있다.
결과적으로 얻은 두 물질의 용량-반응 곡선은 프로피오닐콜린의 곡선이 그의 낮은 효력으로 인해 아세틸콜린의 곡선에 비하여 오른쪽으로 이동되어 있을 뿐 그 형태가 매우 유사함을 알 수 있다. 이 그림에서 우리는 프로피오닐콜린의 효력이 모든 용량 하에서 아세틸콜린의 효력보다 20 이라는 일정한 비율(logarithm scale로 1.3 unit)로 저하되어 있음을 쉽게 알 수 있다. 이와 같은 이점이 있기 때문에 약리학자들은 약리실험의 결과를 그래프로 표시할 때 log 용량-반응곡선을 즐겨 사용하고 있다.
효능약(agonist)과 길항약(antagonist)
금세기 초에 독일의 화학자 Ehrlich는 세포의 일부에는 특정한 구조의 외부 물질(약물)과 화학적 결합을 할 수 있는 부분(작용부위)이 존재하며, 이것이 체내로 들어온 물질(약품)과 결합함으로써 생리적 반응을 유발한다고 주장하였다. 이것이 오늘날 수용체 이론의 기초가 되었는데, 간단히 말해서 생리작용을 분자수준에서 검토할때, 약물은 체내 세포의 표면에 존재하는 일정한 구조와 형태를 가진 물질과 물리,화학적 작용을 통하여 세포 내에서의 생화학적 변화를 유발하고, 결과적으로 거시적인 생리반응으로 발전한다는 것이다. 여기서 약물분자와 결합하는 그 특정한 물질을 수용체 (receptor) 라 부른다. 약물은 수용체와 결합하여 약물-수용체의 복합체를 형성하는데 이 반응은 가역적 반응으로 일반적 화학반응과 같이 질량작용의 법칙을 따른다.

여기서 약물과 수용체간의 결합 용이도를 친화력 (affinity) 이라고 부른다. 그리고 결합의 결과로 유발되는 생리 효과를 효능 (efficacy) 이라고 하고, 그 나타나는 반응을 항진작용(亢進作用, agonistic action) 이라 하며 , 이러한 항진 작용을 소유한 물질을 활성물질 또는 효능약(效能藥)이라고 한다. 그러나 어떤 물질은 그 수용체에 대하여 친화성이 있어 결합을 이루기는 하나 생리효과는 나타내지 못할 뿐만 아니라 효능약의 결합까지도 방해하는 것이 있는데 이런 물질을 길항제(持抗劑 antagonist) 또는 길항약이라 부른다. 예를 들면, 아세틸콜린은 근육의 콜린 수용체와 작용하여 항진적 작용인 근육의 수축을 초래하는데 반하여, d-tubocurarine 와 같은 물질은 그 수용체에 작용하여 아세틸콜린의 항진적 작용을 방해한다. 즉, d-tubocurarine 은 콜린 수용체에 대하여 길항제적 성능을 가지고 있다.


댓글