1. 탄산염이 염산과 반응해 발생하는 이산화탄소의 양을 측정해서 탄산염의 종류를 알아낸다.
2. 대부분의 기체가 높은 온도와 낮은 압력 상태에서는 이상 기체 상태 방정식 PV=nRT을 잘 잘 만족시킨다는 사실을 이용하여 CO2 기체의 압력, 부피, 몰수와 온도를 측정하여 기체상수(R)를 결정하고 미지의 탄산염을 분석한다.
실험실에서 얻은 측정값에는 언제나 불확실도가 포함되기 마련이다. 불확실도는 실험을 여러 차례 반복해서 얻은 측정값을 통계적으로 처리해서 짐작한다. 그러나 실험에 따라서는 불확실도의 크기를 미리 알 수 있는 경우도 있다. 예를 들어서 어림 저울을 사용하는 경우에는 저울의 가장 작은 눈금의 1/10 보다 작은 값을 얻을 수 있다. 온도나 압력과 같은 외부적인 측정값에 영향을 미치는 경우도 있다.
측정값에 영향을 주는 요인을 미리 알아내어 이를 측정값에 적정하게 반영시켜주는 과정을 측정값의 보정(calibration)이라고 한다. 그러나 실험에 따라서는 모든 불확실도의 요인을 미리 파악해서 측정값에 반영시켜줄 필요가 없는 경우도 있다. 측정값에 대한 보정이 필요한가 그렇지 않은가는 실험에서 궁극적으로 얻으려고 하는 결과의 정확도가 얼마인가에 따라서 결정된다. 매우 정확한 결과를 얻기 위해서는 실험과정에 포함된 모든 측정값들이 정확해야 하고, 따라서 측정에 영향을 미칠 수 있는 모든 요인을 파악하고, 필요한 경우에는 측정값들을 적절하게 보정해 주어야한다.
그러나 실험 결과의 불확실도 범위에 들어갈 정도로 영향이 작은 불확실도의 요인은 고려하지 않는 것이 실험 시간과 비용을 절약하는 방법이 된다. 측정에 미치는 불확실도의 요인이 실험 결과에 어떤 영향을 미치는가를 알아내기 위해서는 측정하려고 하는 물리적 양의 의미와 측정 방법에 대한 광범위한 지식이 필요하며, 그런 지식은 실험을 통해서 얻을 수밖에 없다.
본 실험에서는 알칼리 금속의 탄산염에 염산을 넣을 때 발생하는 이산화탄소 기체의 양을 측정해서 알칼리 금속의 종류를 알아내는 과정을 통하여 측정에 영향을 줄 수 있는 불확실도 요인을 파악하고, 알칼리 금속의 종류를 알아내려는 실험의 목적을 고려할 때 어떤 불확실도 요인이 영향을 미칠 것인가를 알아본다. 알칼리 금속 M(Li, Na, K, Rb, Cs, Fr)은 M2CO3 형태의 탄산염을 형성하는데, 알칼리 금속의 탄산염을 묽은 염산에 넣어주면 이산화탄소가 발생한다. 주어진 무게의 탄산염에서 얻어진 이산화탄소의 양을 알아내면 알칼리 금속 M의 종류를 알아낼 수 있다.
M2CO3 + 2HCl → 2M+ + Cl- + H2O + CO2
알칼리 금속의 탄산염이 염산과 반응할 때 발생하는 기체의 부피는 물을 채운 유리관을 이용해서 측정한다. 기체의 부피를 측정하기 위한 목적으로 제작된 측기관(eudometer)을 사용할 수도 있지만, 이 실험에서는 물을 채운 유리관을 거꾸로 세워서 측기관으로 사용한다. 이산화탄소 기체의 부피를 측정하는 과정에 영향을 미칠 수 있는 불확실도의 요인을 정확하게 파악하고, 그런 불확실도가 알칼리 금속의 종류를 알아내는 데에 어떤 영향을 미칠 것인가를 알아보는 것이 이 실험의 목적이다.
실험 방법
1. 실험 과정
1) 그림과 같이 실험 장치를 꾸민다.
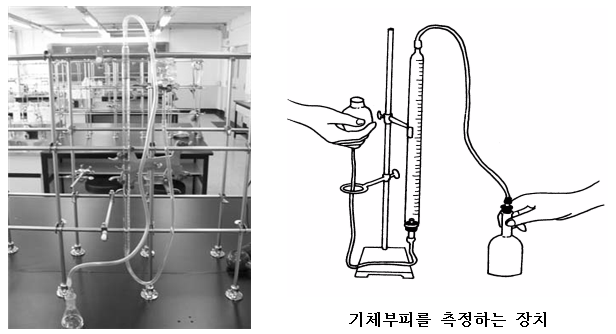
2) 타이곤튜브를 이용하여 100㎖ 피펫의 아랫쪽에는 수위조절기를 연결하고 위쪽은 adaptor와 연결한 후 피펫의 수위를 0㎖ 근처에 오도록 증류수를 채운다.
3) 후드에서 3M HCl을 100㎖ volumetric flask를 이용하여 만든다.
4) 알칼리금속에 해당하는(Li2CO3, Na2CO3, K2CO3) 중의 하나를 선택해서 미지 시료로 사용한다
5) 미지시료 I, II를 대략 0.25을 vial cap에 각각 담아 무게를 정확하게 잰다.
6) 물로 기체부피 측정장치를 만들고 물의 온도를 측정한다.
7) 100㎖ 삼각플라스크(Erlenmeyer flask)에 3M HCl 40㎖를 넣고 미지시료 I이 담긴 vial cap을 핀셋으로 조심스럽게 HCl용액 위에 띄워놓는다.
8) 25㎖ 피펫의 아래쪽에 수위 조절기를 연결하고, 위쪽은 플라스크와 연결한 후, 유리관의 물높이를 가장 높은 눈금 부근에 오도록 조절한다.
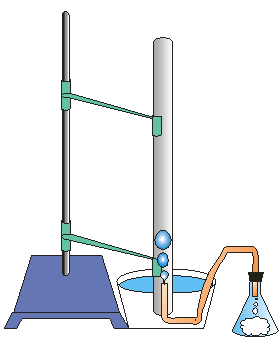
9) Vacuum adaptor로 삼각플라스크(Erlenmeyer flask)의 입구를 막는다. 기체가 샐 수 있는 부분을 파라필름으로 잘 막는다.
10) 삼각플라스크(Erlenmeyer flask)를 조금씩 흔들어 주면서 반응을 시킨다. 이때 너무 과격하게 흔들면 미지시료 I 이 벽면에 튀어서 반응을 안 할 수 있으니 조심한다.
11) 플라스크를 조금씩 흔들어주면서 반응을 시킨다. 이산화탄소가 발생되기 시작하면 수위조절기를 낮추어 피펫과 수위조절기의 수위를 맞춰준다.
12) 더 이상 기체가 발생하지 않으면 수위조절기의 높이를 피펫의 수위와 정확히 맞춘 후 눈금을 읽고 기록한다.
13) 실험실의 온도와 압력을 기록한다.
14) 위의 과정을 반복하여 미지시료 I, II 에 대하여 각각 2개의 데이터를 얻는다.
15) 각각 두 개의 데이터 평균을 구하여 미지의 탄산염 I, II 을 결정한다.
[일반화학실험]탄산염의 분석 1부
[일반화학실험]탄산염의 분석 1부...
educhemup.blogspot.com
[일반화학실험]탄산염의 분석 레포트
실험실에서 얻은 측정값에는 언제나 불확실도가 포함되기 마련이다. 불확실도는 실험을 여러 차례 반복해서 얻은 측정값을 통계적으로 처리해서 짐작한다. 그러나 실험에 따라서는 불확실도의 크기를 미리 알 수 있는 경우도 있다. 예를 들어서 어림 저울을 사용하는 경우에는 저울의 가장 작은 눈금의 1/10 보다 작은 값을 얻을 수 있다. 온도나 압력과 같은 외부적인 측정값에 영향을 미치는 경우도 있다. 측정값에 영향을 주는 요인을 미리 알아내어 이를 측정값에 적정하...
www.happycampus.com


댓글