
분자들로 존재하는 화합물들은 그 분자 내에 있는 각종 원자의 수를 나타내는 화학식(chemical formulas)으로 표시한다. 예를 들면 당인 글루코오스는 6개의 탄소 원자와 12개의 수소 원자 그리고 6개의 산소 원자를 포함하므로 이의 화학식은 C6H12O6이다. H2, N2, O2, Cl2, P4, 또는 S8과 같이 유리상태로 존재하는 원소들은 다원자 분자로 존재한다. 어떤 화합물의 화학식과 그 구성원소의 원자량을 알면 그 화합물에 있는 원소의 조성백분율을 계산할 수 있다. 구성원소의 백분율은 화학식에 포함된 그 원소의 총 원자량을 화학식량으로 나누고 100을 곱하면 된다.
실험식
실험식(empirical formulas)은 가장 간단한 식이며 가능한 한 가장 간단한 방법으로 원소 분석 결과를 나타낸 것이다. 실험식은 단지 화합물을 구성하는 각 원소의 상대적 원자수만을 나타낸다. 이 식은 화학물의 실제 분자식에 해당할 때도 있고 그렇지 않을 때도 있다. 화합물의 실험식은 화합물 속에 들어 있는 각 원소에 대한 원자의 상대적 몰수를 결정하여 나타낸 식이다. 시료 속에 존재하는 각 원소의 몰수비는 이들 원소의 원자수비와 같다.
분자식
분자식(molecular formulas)은 분자의 정확한 원자 조성을 나타낸 화학식이다. 즉 실험식은 화합물 속에 있는 각 원소의 원자들의 상대적인 수만을 나타내지만, 분자식은 원자들의 실제적인 수를 나타낸다. 분자식은 실험에 필요한 많은 화학정보를 제공한다. 분자식은 실험식이 같으나 물질이 서로 다른 것들을 구분하는데 도움을 준다. 예를 들면 아세틸렌과 벤젠은 실험식이 같지만(CH) 아세틸렌의 분자식은 C2H2이고 벤젠의 분자식은 C6H6이다. 분자형태로 존재하는 물질의 분자식과 실험식의 구별은 그 분자량으로부터 추정할 수 있다. 분자량은 일정량의 질량 속에 존재하는 분자수를 결정함으로써 알 수 있다.
실험식은 화학 조성만 알면 계산해낼 수 있지만, 분자식은 실험식으로부터 알아낼 수 없다. 분자식은 분자량과 그 실험식에 해당하는 화학식량을 비교하여 결정할 수 있다. X-선 회절(X-ray diffraction)에 의한 방법과 같이 직접 분자 구조를 확인하는 방법으로도 분자식을 알 수 있다. 분자식을 적을 때는 집합상태(states of aggregation)를 괄호 속에 적어 넣을 수도 있다. 예를 들면 기체 브롬, 액체 브롬, 고체 브롬을 각각 Br2(g), Br2(l), Br2(s)로 나타낸다. 또한 이와 유사한 것으로 Al3+(aq) 혹은 Cl2(aq)에서와 같이 수용액을 이루는 화학종은 (aq) 표시로 나타낸다.
구조식
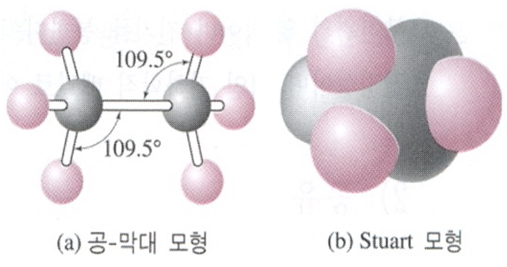
구조식(structural formulas)은 어떤 화합물의 원자 배열에 대한 상세한 정보를 준다. 따라서 분자 내에서의 원자의 결합상태, 결합순서 그리고 분자의 형태 등을 알아볼 수 있다(그림 1 참조). 에탄올(CH3CH2OH)과 디메틸에테르(CH3OCH3)는 C2H6O의 같은 분자식을 갖고 있다. 그러나 이 둘은 서로 다른 분자 구조를 갖고 물리적 화학적 성질이 다른 물질들이다. 이와 같이 분자식은 같지만 구조나 성질 등이 다른 화합물들을 이성질체(isomer)라고 한다.
[Chemistry/생활 속 화학] - 화학 이론 | 화학의 영역
[Chemistry/생활 속 화학] - 화학 이론 | 원자
[Chemistry/생활 속 화학] - 화학 이론 | 주기율 표
[Chemistry/생활 속 화학] - 화학 이론 | 전자배치
[Chemistry/생활 속 화학] - 화학 이론 | 분자와 이온
[Chemistry/생활 속 화학] - 화학 이론 | 화학 결합
[Chemistry/생활 속 화학] - 화학 이론 | 산화와 환원
[Chemistry/생활 속 화학] - 화학 이론 | 액체와 용액
[Chemistry/생활 속 화학] - 화학 이론 | 산과 염기 1부
[일반화학]화학의 이론 레포트
1. 화학의 영역 화학이란 물체의 구성이나 성질 및 구조에 대하여 연구하는 학문이다. 어떤 물체는 하나 또는 그 이상의 화학원소로 이루어져 있다. 원소(element)란 화학반응에 의하여 간단한 형태로 더 이상 분해되지 않는 물체의 한 형태이다. 현재 100개가 넘는 원소들이 알려져 있으며 한 원소는 다른 원소들과 구별되는 고유한 특성이 있다. 각 원소의 기호(symbol)는 주로 영어나 라틴어의 약자로 표시되었고, 이 기호는 원소의 원자를 표시하는데 사
www.happycampus.com


댓글